Yksi tärkeimmistä kysymyksistä fysiikan termodynaamisten järjestelmien tutkimuksessa on kysymys siitä, voiko tämä järjestelmä suorittaa jotain hyödyllistä työtä. Työn käsitteeseen liittyy läheisesti sisäisen energian käsite. Tässä artikkelissa pohditaan, mikä on ihanteellisen kaasun sisäenergia ja annamme kaavat sen laskemiseen.
Ihanteellinen kaasu
Kaasusta aggregaatiotilana, jolla ei ole ulkoisen vaikutuksen alaisena elastista voimaa ja jonka seurauksena se ei säilytä tilavuutta ja muotoa, jokainen koululainen tietää. Ideaalikaasun käsite monille on edelleen käsittämätön ja epäselvä. Selitetään se.
Ihanteellinen kaasu on mikä tahansa kaasu, joka täyttää seuraavat kaksi tärkeää ehtoa:
- Sen muodostavilla hiukkasilla ei ole kokoa. Niillä on koko, mutta se on niin pieni niiden välisiin etäisyyksiin verrattuna, että se voidaan jättää huomiotta kaikissa matemaattisissa laskelmissa.
- Hartikkelit eivät ole vuorovaikutuksessa toistensa kanssa käyttämällä van der Waalsin voimia tai voimiamuu luonto. Itse asiassa kaikissa todellisissa kaasuissa tällainen vuorovaikutus esiintyy, mutta sen energia on mitätön verrattuna kineettisten hiukkasten keskimääräiseen energiaan.
Kuvatut ehdot täyttävät lähes kaikki todelliset kaasut, joiden lämpötilat ovat yli 300 K ja paineet eivät ylitä yhtä ilmakehää. Liian korkeissa paineissa ja matalissa lämpötiloissa havaitsee kaasujen poikkeaman ihanteellisesta käyttäytymisestä. Tässä tapauksessa puhutaan todellisista kaasuista. Ne kuvataan van der Waalsin yhtälöllä.
Ideaalikaasun sisäisen energian käsite
Määritelmän mukaan järjestelmän sisäinen energia on tämän järjestelmän sisältämien kineettisten ja potentiaalisten energioiden summa. Jos tätä käsitettä sovelletaan ihanteelliseen kaasuun, mahdollinen komponentti on hylättävä. Itse asiassa, koska ihanteellisen kaasun hiukkaset eivät ole vuorovaikutuksessa toistensa kanssa, niiden voidaan katsoa liikkuvan vapaasti absoluuttisessa tyhjiössä. Yhden hiukkasen erottamiseksi tutkittavasta järjestelmästä ei tarvitse tehdä työtä sisäisiä vuorovaikutusvoimia vastaan, koska näitä voimia ei ole olemassa.
Täten ihanteellisen kaasun sisäinen energia on aina sama kuin sen liike-energia. Jälkimmäinen puolestaan määritetään yksiselitteisesti järjestelmän hiukkasten moolimassan, niiden lukumäärän sekä translaatio- ja pyörimisliikkeen keskimääräisen nopeuden perusteella. Liikkeen nopeus riippuu lämpötilasta. Lämpötilan nousu johtaa sisäisen energian kasvuun ja päinvastoin.
Formula forsisäinen energia
Ilmoita ihanteellisen kaasujärjestelmän sisäenergiaa U-kirjaimella. Termodynamiikan mukaan se määritellään erotuksena järjestelmän entalpian H ja paineen ja tilavuuden tulon välillä, eli:
U=H - pV.
Yllä olevassa kappaleessa havaitsimme, että U:n arvo vastaa kaikkien kaasuhiukkasten liike-energiaa Ek:
U=Ek.
Tilastollisesta mekaniikasta ihanteellisen kaasun molekyylikineettisen teorian (MKT) puitteissa seuraa, että yhden hiukkasen keskimääräinen kineettinen energia Ek1 on yhtä suuri kuin seuraava arvo:
Ek1=z/2kBT.
Tässä kB ja T - Boltzmannin vakio ja lämpötila, z - vapausasteiden lukumäärä. Järjestelmän kokonaiskineettinen energia Ek saadaan kertomalla Ek1 järjestelmän hiukkasten lukumäärällä N:
Ek=NEk1=z/2NkBT.
Täten olemme saaneet ihanteellisen kaasun sisäisen energian kaavan, joka on kirjoitettu yleisessä muodossa absoluuttisen lämpötilan ja hiukkasten lukumäärän suhteen suljetussa järjestelmässä:
U=z/2NkBT.
Monatominen ja moniatominen kaasu
Artikkelin edellisessä kappaleessa kirjoitettu kaava U:lle on hankala käytännön käytössä, koska hiukkasten N määrää on vaikea määrittää. Jos kuitenkin otamme huomioon aineen n määrän määritelmän, tämä lauseke voidaan kirjoittaa uudelleen kätevämpään muotoon:
n=N/NA; R=NAkB=8, 314 J/(molK);
U=z/2nR T.
Vapausasteiden lukumäärä z riippuu kaasun muodostavien hiukkasten geometriasta. Siten yksiatomiselle kaasulle z=3, koska atomi voi liikkua itsenäisesti vain kolmeen avaruuden suuntaan. Jos kaasu on diatominen, niin z=5, koska kolmeen translaatiovapausasteeseen lisätään vielä kaksi rotaatiovapausastetta. Lopuksi minkä tahansa muun polyatomisen kaasun os alta z=6 (3 translaatio- ja 3 rotaatiovapausastetta). Tätä silmällä pitäen voimme kirjoittaa seuraavassa muodossa kaavat yksiatomisen, kaksiatomisen ja moniatomisen ideaalikaasun sisäiselle energialle:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
Esimerkki tehtävästä sisäisen energian määrittämiseksi
100 litran sylinteri sisältää puhdasta vetyä 3 ilmakehän paineessa. Jos oletetaan, että vety on ihanteellinen kaasu tietyissä olosuhteissa, on tarpeen määrittää sen sisäinen energia.

Yllä olevat U:n kaavat sisältävät aineen määrän ja kaasun lämpötilan. Ongelmatilanteessa näistä määristä ei puhuta mitään. Ongelman ratkaisemiseksi on muistettava yleinen Clapeyron-Mendeleev-yhtälö. Sen ulkonäkö on kuvan mukainen.
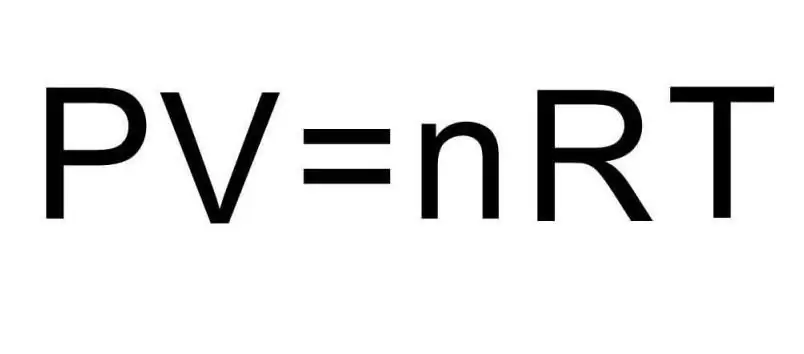
Koska vety H2 on kaksiatominen molekyyli, sisäisen energian kaava on:
UH2=5/2nRT.
Vertaamalla molempia lausekkeita pääsemme lopulliseen ongelman ratkaisukaavaan:
UH2=5/2PV.
Enää on muutettava paineen ja tilavuuden yksiköt ehdosta SI-yksikköjärjestelmään, korvattava vastaavat arvot kaavassa UH2 ja saadaan vastaus: UH2 ≈ 76 kJ.






