Ideaalikaasun ominaisuuksien tutkiminen on tärkeä aihe fysiikassa. Johdatus kaasujärjestelmien ominaisuuksiin alkaa Boyle-Mariotte-yhtälön tarkastelulla, koska se on ensimmäinen kokeellisesti löydetty ihanteellisen kaasun laki. Pohditaanpa sitä yksityiskohtaisemmin artikkelissa.
Mitä ihanteellinen kaasu tarkoittaa?
Ennen kuin puhumme Boyle-Mariotten laista ja sitä kuvaavasta yhtälöstä, määritellään ihanteellinen kaasu. Se ymmärretään yleisesti nestemäiseksi aineeksi, jossa sen muodostavat hiukkaset eivät ole vuorovaikutuksessa toistensa kanssa ja niiden koot ovat mitättömän pieniä verrattuna keskimääräisiin hiukkasten välisiin etäisyyksiin.
Itse asiassa mikä tahansa kaasu on todellista, eli sen muodostavilla atomeilla ja molekyyleillä on tietty koko, eivätkä ne ole vuorovaikutuksessa toistensa kanssa van der Waalsin voimien avulla. Kuitenkin korkeissa absoluuttisissa lämpötiloissa (yli 300 K) ja matalissa paineissa (alle yksi ilmakehä) atomien ja molekyylien kineettinen energia on paljon suurempi kuin van der Waalsin vuorovaikutusten energia, joten todellinen kaasu ilmoitetussaolosuhteita suurella tarkkuudella voidaan pitää ihanteellisina.
Boyle-Mariotten yhtälö
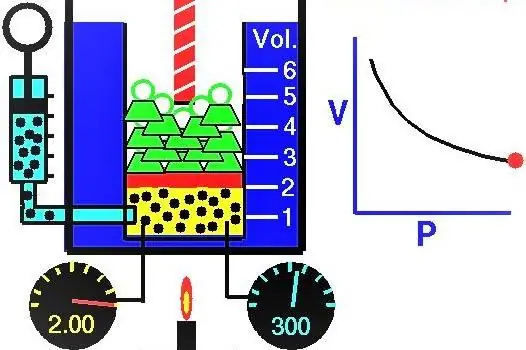
Kaasujen ominaisuudet Eurooppalaiset tiedemiehet tutkivat aktiivisesti XVII-XIX vuosisatojen aikana. Ensimmäinen kokeellisesti löydetty kaasulaki oli laki, joka kuvaa kaasujärjestelmän isotermisiä laajenemis- ja puristusprosesseja. Vastaavat kokeet suorittivat Robert Boyle vuonna 1662 ja Edm Mariotte vuonna 1676. Jokainen näistä tutkijoista osoitti itsenäisesti, että suljetussa kaasujärjestelmässä tapahtuvan isotermisen prosessin aikana paine muuttuu käänteisesti tilavuuden kanssa. Prosessin kokeellisesti saatu matemaattinen lauseke kirjoitetaan seuraavassa muodossa:
PV=k
Missä P ja V ovat järjestelmän paine ja tilavuus, k on jokin vakio, jonka arvo riippuu kaasuaineen määrästä ja sen lämpötilasta. Jos rakennat P(V)-funktion riippuvuuden kaavioon, se on hyperbola. Esimerkki näistä käyristä on esitetty alla.
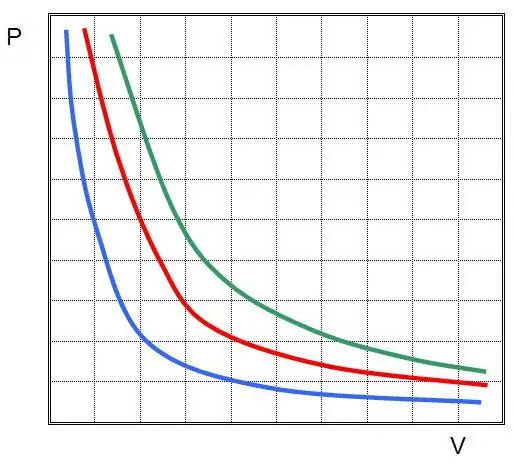
Kirjoitettua yhtälöä kutsutaan Boyle-Mariotten yhtälöksi (laki). Tämä laki voidaan muotoilla lyhyesti seuraavasti: ihanteellisen kaasun laajeneminen vakiolämpötilassa johtaa suhteelliseen paineen laskuun siinä, päinvastoin, kaasujärjestelmän isotermiseen puristumiseen liittyy suhteellinen paineen nousu siinä.
Ihanteellinen kaasuyhtälö
Boyle-Mariotten laki on erikoistapaus yleisemmälle laille, joka kantaa Mendelejevin jaClapeyron. Emile Clapeyron, tiivistämällä kokeelliset tiedot kaasujen käyttäytymisestä erilaisissa ulkoisissa olosuhteissa, sai vuonna 1834 seuraavan yhtälön:
PV=nRT
Toisin sanoen kaasujärjestelmän tilavuuden V ja siinä olevan paineen P tulo on suoraan verrannollinen absoluuttisen lämpötilan T ja aineen n määrän tuloon. Tämän suhteellisuuskerroin on merkitty kirjaimella R ja sitä kutsutaan kaasun yleisvakioksi. Kirjatussa yhtälössä R:n arvo ilmestyi useiden vakioiden korvaamisen vuoksi, jonka teki Dmitri Ivanovitš Mendelejev vuonna 1874.
Universaalisesta tilayhtälöstä on helppo nähdä, että lämpötilan ja aineen määrän vakioisuus takaa yhtälön oikean puolen invarianssin, mikä tarkoittaa, että yhtälön vasen puoli pysyy myös vakiona. Tässä tapauksessa saamme Boyle-Mariotten yhtälön.

Muut kaasulait
Yllä olevassa kappaleessa kirjoitettu Clapeyron-Mendeleev-yhtälö sisältää kolme termodynaamista parametria: P, V ja T. Jos jokainen niistä on kiinteä ja kahden muun annetaan muuttua, saadaan Boyle-Mariotte, Charlesin ja Gay-Lussacin yhtälöt. Charlesin laki puhuu isobarisen prosessin tilavuuden ja lämpötilan suorasta suhteesta, ja Gay-Lussacin laki sanoo, että isokorisen siirtymän tapauksessa kaasun paine kasvaa tai laskee suoraan suhteessa absoluuttiseen lämpötilaan. Vastaavat yhtälöt näyttävät tältä:
V/T=const kun P=const;
P/T=const, kun V=const.
JotenNäin ollen Boyle-Mariotten laki on yksi kolmesta kaasulakista. Se eroaa kuitenkin muista graafisen riippuvuuden suhteen: funktiot V(T) ja P(T) ovat suoria viivoja, funktio P(V) on hyperbola.
Esimerkki tehtävästä Boyle-Mariotten lain soveltamiseksi
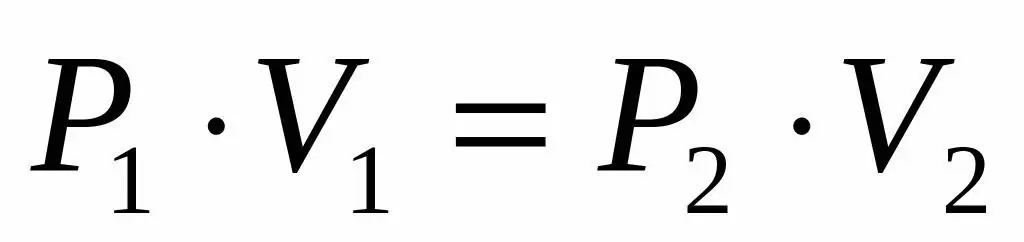
Kaasun tilavuus männän alla olevassa sylinterissä alkuasennossa oli 2 litraa ja sen paine oli 1 ilmakehä. Mikä oli kaasun paine sen jälkeen, kun mäntä nousi ja kaasujärjestelmän tilavuus kasvoi 0,5 litraa. Prosessia pidetään isotermisenä.
Koska meille on annettu ihanteellisen kaasun paine ja tilavuus ja tiedämme myös, että lämpötila pysyy muuttumattomana sen laajenemisen aikana, voimme käyttää Boyle-Mariotte-yhtälöä seuraavassa muodossa:
P1V1=P2V 2
Tämä yhtälö sanoo, että tilavuus-painetulo on vakio jokaisessa kaasun tilassa tietyssä lämpötilassa. Ilmaisemalla arvon P2 yhtäläisyydestä saadaan lopullinen kaava:
P2=P1V1/V 2
Painelaskelmia tehdessäsi voit tässä tapauksessa käyttää järjestelmän ulkopuolisia yksiköitä, koska litrat kutistuvat ja saadaan paine P2ilmakehissä. Korvaamalla tiedot ehdosta saadaan vastaus ongelman kysymykseen: P2=0,8 ilmakehää.






