Koduktometrinen analyysimenetelmä on elektrolyyttisen johtavuuden mittaaminen kemiallisen reaktion etenemisen seuraamiseksi. Tätä tiedettä käytetään laajasti analyyttisessä kemiassa, jossa titraus on vakiotoimintamenetelmä. Mikä on konduktometria? Analyyttisen kemian yleisessä käytännössä termiä käytetään synonyyminä titraamiselle, mutta sitä käytetään myös kuvaamaan ei-titraussovelluksia. Mitä hyötyä tämän analyysimenetelmän käytöstä on? Sitä käytetään usein määrittämään liuoksen kokonaisjohtavuus tai analysoimaan ioneja sisältävän titrauksen päätepiste.
Historia
Johtavat mittaukset alkoivat jo 1700-luvulla, kun Andreas Baumgartner huomasi, että Bad Gasteinin suola- ja kivennäisvedetItäv alta johtaa sähköä. Näin ollen tämän menetelmän käyttö veden puhtauden määrittämiseen, jota nykyään käytetään usein vedenpuhdistusjärjestelmien tehokkuuden testaamiseen, alkoi vuonna 1776. Näin alkoi konduktometrisen analyysimenetelmän historia.
Friedrich Kohlrausch jatkoi tämän tieteen kehittämistä 1860-luvulla, kun hän käytti vaihtovirtaa veteen, happoihin ja muihin liuoksiin. Noihin aikoihin rikkihapon ja kromisulfaattikompleksien vuorovaikutuksia tutkiva Willis Whitney löysi ensimmäisen konduktometrisen päätepisteen. Nämä havainnot huipentuivat potentiometriseen titraukseen ja Robert Behrendin ensimmäiseen volumetriseen analyysiin vuonna 1883 kloridin ja bromidin HgNO3 titraamiseen. Siten nykyaikainen konduktometrinen analyysimenetelmä perustuu Behrendiin.
Tämä kehitys mahdollisti suolojen liukoisuuden ja vetyionien pitoisuuden sekä happo-emäs- ja redox-titrausten testaamisen. Konduktometristä analyysimenetelmää parannettiin lasielektrodin kehittämisen myötä, joka alkoi vuonna 1909.
Titraus
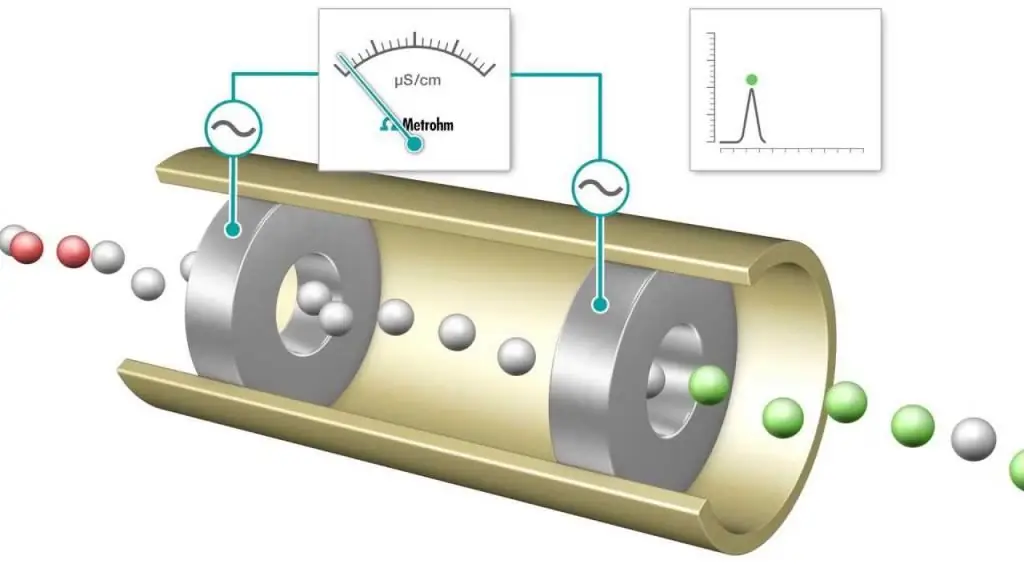
Konduktometrinen titraus on mittaus, jossa reaktioseoksen elektrolyyttistä johtavuutta seurataan jatkuvasti lisäämällä yhtä reagenssia. Ekvivalenssipiste on piste, jossa johtavuus yhtäkkiä muuttuu. Johtavuuden huomattava lisääntyminen tai lasku liittyy kahden eniten johtavan ionin, vety- ja hydroksidi-ionin, pitoisuuden muutokseen. Tämä menetelmävoidaan käyttää värillisten liuosten tai homogeenisten suspensioiden (esim. puumassasuspension) titraamiseen, joita ei voida käyttää tavanomaisten indikaattoreiden kanssa.
Happo-emäs- ja redox-titrauksia suoritetaan usein, joissa käytetään yhteisiä indikaattoreita päätepisteen määrittämiseen, kuten metyylioranssi, fenolftaleiini happo-emäs-titraukseen ja tärkkelysliuoksia jodometrisen tyyppiseen redox-prosessiin. Sähkönjohtavuusmittauksia voidaan kuitenkin käyttää myös työkaluna päätepisteen määrittämiseen, esimerkiksi tarkasteltaessa HCl-liuosta, jossa on vahva emäs NaOH.
Protonineutralointi
Titrauksen edetessä protonit neutraloidaan muodostaen NaOH:ta muodostamalla vettä. Jokaista lisättyä NaOH-määrää kohden poistetaan vastaava määrä vetyioneja. Käytännössä liikkuva H+-kationi korvataan vähemmän liikkuvalla Na+-ionilla ja titratun liuoksen johtavuus sekä mitattu solun johtavuus pienenevät. Tätä jatketaan, kunnes saavutetaan ekvivalenssipiste, jossa natriumkloridi-NaCl-liuos voidaan saada. Jos emästä lisätään enemmän, se lisääntyy, kun enemmän Na+- ja OH--ioneja lisätään, eikä neutralointireaktio enää poista huomattavaa määrää H+:a.

Jos näin ollen, kun vahva happo titrataan vahvalla emäksellä, johtavuus on minimissään ekvivalenssipisteessä. Tämä minimivoidaan käyttää indikaattorivärin sijasta titrauksen päätepisteen määrittämiseen. Titrauskäyrä on kaavio johtavuuden tai johtavuuden mitatuista arvoista lisätyn NaOH-liuoksen tilavuuden funktiona. Titrauskäyrää voidaan käyttää ekvivalenssipisteen graafiseen määrittämiseen. Konduktometrinen analyysimenetelmä (ja sen käyttö) on erittäin tärkeä nykyajan kemiassa.
Reaktio
Heikon happo-heikon emäksen välisessä reaktiossa sähkönjohtavuus laskee ensin jonkin verran, koska käytettävissä olevia H+-ioneja käytetään vähän. Sitten johtavuus kasvaa hieman ekvivalenssipisteen tilavuuteen asti suolakationin ja anionin vaikutuksesta (tämä osuus vahvan happaman emäksen tapauksessa on mitätön, eikä sitä oteta huomioon.) Kun ekvivalenssipiste on saavutettu, johtavuus kasvaa nopeasti OH-ionien ylimäärän vuoksi.
Johtavuusilmaisimia (konduktometrinen analyysimenetelmä) käytetään myös elektrolyyttipitoisuuksien mittaamiseen vesiliuoksissa. Liuoksen johtavuuden muodostavan analyytin molaarinen pitoisuus saadaan liuoksen mitatusta sähkövastuksesta.
Konduktometrinen analyysimenetelmä: periaate ja kaavat
(2.4.13) C=Constcell1Λm1Res, jossa Constcell on vakioarvo mittakennosta riippuen, Res on laitteen mittaama sähkövastus (ohmin lain mukaan Res=I / V ja vakiolla jännitteen V mittaus I intensiteetti antaa sinun laskea Res), ja Λm on ekvivalenttiionihiukkasten johtavuus. Vaikka käytännön syistä Λm:ä voidaan pitää vakiona, se riippuu pitoisuudesta Kohlrauschin lain mukaan:
(2.4.14)=Хт Λm0-ΘC, missä Θ on vakio ja Λm0 on kunkin ionin rajoittava molaarinen johtavuus. Molaarinen johtavuus puolestaan riippuu lämpötilasta.
Scrit
Mittausanalyysin konduktometrisen menetelmän kehitys on johtanut tutkijat uusiin löytöihin. Tiedemiehet määrittelivät kriittisen ylikyllästyssuhteen, Scrit, käyttämällä konduktiometriaa homogeenisessa AgCl-saostusjärjestelmässä yli Ag+-ionien kanssa käyttämällä alkyylikloridihydrolyysiä CI-ionien lähteenä. He löysivät Scrit=1,51, 1,73 ja 1,85 vastaavasti 15, 25 ja 35 °C:ssa, missä S=([Ag+][Cl-] / Ksp) 1/2 niiden määritelmän mukaan. Jos tämä ylikyllästystekijän määritelmä muunnetaan omaksi (S=[Ag+][Cl-] / Ksp), tulokset ovat 2,28, 2,99 ja 3,42, mikä on melko hyvin sopusoinnussa tämän tutkimuksen tulosten kanssa. Scritin lämpötilariippuvuus on kuitenkin päinvastainen kuin tässä tutkimuksessa kuvattu. Vaikka tämän ristiriidan syy ei ole selvä, Scrit:n lasku lämpötilan noustessa voi olla varsin järkevää, koska ytimen muodostumisnopeus muuttuu dramaattisesti pienellä ΔGm/ kT:n ja siten ΔGm/ kT:n muutoksella, joka on verrannollinen T:hen. − 3 (lnSm) 2:n kaavan (1.4.12) mukaan katsotaan olevan lähes vakio lämpötilan muutoksen kanssa tietyssä järjestelmässä. Muuten, S:n määritelmän on oltava [Ag +] [Cl -] / Ksp, koska ylikylläisyyssuhde suhteessa[AgCl]-monomeeripitoisuus annetaan aluksi muodossa S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp.
Tanaka ja Iwasaki
Kaksi ikonista japanilaista tiedemiestä jatkoi konduktometrisen analyysimenetelmän historiaa. Tanaka ja Iwasaki tutkivat AgCl- ja AgBr-hiukkasten nukleaatioprosessia pysäytysvirtausmenetelmällä yhdistettynä monikanavaiseen spektrofotometriin, joka on hyödyllinen nopean prosessin tutkimiseen ms luokkaa. He havaitsivat, että jokin spesifinen hopeahalogenidikompleksi AgXm (m-1), jolla oli melko kapea UV-absorptiokaista, muodostui välittömästi, kun AgC104-liuosta, jonka luokka oli 10-4 mol dm-3, sekoitettiin KX:n kanssa (X=Cl tai Br) liuos, jonka suuruusluokka on 10-2 - 10-1 mol dm-3, mitä seuraa sen nopea hajoaminen noin 10 ms, jolloin muodostuu välituote, jolla on laaja UV-absorptio ja paljon hitaampi spektrin muutos. välituotteesta. He tulkitsevat välituotteen monodisperssiksi ytimeksi (AgX) n, jotka koostuivat n molekyylistä ja määrittelivät n näennäissuhteesta -dC/dt α Cn, kun t=0 C-prekursorin AgXm eri alkupitoisuuksille (m-1) - (n=7) -10 AgCl:lle, n=3-4 AgBr:lle).

Koska prekursori AgXm (m − 1) kuitenkin hajoaa ei-stationaarisesti, kvasistationaarisen ydintymisen teoria ei päde tässä prosessissa, joten tuloksena oleva n:n arvo ei vastaa nkriittisten ytimien arvo. Jos välituote sisältää monodisperssiä ytimiä,monomeerisen kompleksin muodostama -dC/dt α C -suhde ei välttämättä säily. Ellemme oletamme, että n-meeriä pienemmät klusterit ovat tasapainossa, ki − 1, ici − 1c1=ki, i − 1ci, toistensa kanssa peräkkäisessä reaktiossa c1 → c2 → c3 →… → cn − 1 → cn., ja vain viimeinen askel cn − 1 → cn on irreversiibeli; eli c1⇌c2⇌c3⇌… ⇌cn − 1 → cn.
Lisäksi tulisi olettaa, että klusterien pitoisuuksilla 2 - n-1 on mitättömät tasapainopitoisuudet. Näille olettamuksille ei kuitenkaan näytä olevan perusteita. Toisa alta yritimme laskea kriittisten ytimien säteet ja ylikyllästyskertoimet S nopean prosessin lopussa käyttämällä γ=101 mJ m − 2 kuutio AgCl19:lle ja γ=109 mJ m − 2 kuutiolle AgBr20, olettaen, että arvot n, 7-10 AgCl19:lle ja 3-4 AgBr20:lle, vastaavat monodispersisten ytimien kokoa, n. Konduktometrinen analyysimenetelmä, jonka arvostelut vaihtelevat yksinkertaisesti hyväksymisestä ihailemiseen, synnytti kemian tieteena.
Tämän tuloksena tutkijat löysivät seuraavan kaavan: r=0,451 nm ja S=105 AgCl:lle, jossa n=9; r=0,358 nm ja S=1230 AgBr:lle, jossa n=4. Koska heidän järjestelmänsä ovat verrattavissa Davisin ja Jonesin järjestelmiin, jotka saivat kriittisen AgCl:n ylikyllästyksen noin 1,7-2,0 25 °C:ssa. Käytettäessä suorasekoituskonduktometriaa yhtä suurissa tilavuuksissa laimeita AgNO3:n ja KCl:n vesiliuoksia, erittäin korkeat S-arvot eivät välttämättä heijasta todellisia ylikyllästystekijöitä.tasapainossa väliytimien kanssa.
UV-absorptio
Vaikuttaa järkevämmältä liittää välituote, jolla on laaja UV-absorptio, paljon keskimääräistä suurempiin ytimiin, joilla on laaja kokojakauma, joka syntyy ei-stationaarisen peräkkäisen reaktion seurauksena. Myöhempi väliytimien hidas muutos näyttää liittyvän niiden kypsymiseen Ostwaldissa.

Yllä olevassa yhteydessä amerikkalainen kemisti Nielsen johti myös bariumsulfaattihiukkasten nukleaatiolle samanlaisen n:n noin 12:n ja vastaavan S:n, joka on suurempi kuin 103, sameusmittauksista ylikyllästyksen funktiona käyttämällä n=dlogJ / dlogC Becher-Deringin k altaisessa teoriassa kaavaan. (1.3.37), mutta antaa (n+ 1) n:n sijaan. Koska barium-ionien ja sulfaatti-ionien liuokset sekoitettiin suoraan tässä kokeessa, nopean ohimenevän ydintymisen olisi pitänyt päättyä välittömästi sekoittamisen jälkeen, ja mitattu voi olla hitaan myöhemmän Ostwaldin kypsymisen ja/tai muodostuneiden ytimien fuusionopeus. Ilmeisesti tämä on syy n:n kohtuuttoman pieneen arvoon ja erittäin korkeaan ylikylläisyyteen. Siksi meidän on jälleen huomattava, että jokin monomeeristen lajien säiliö, joka vapauttaa niitä vastauksena niiden kulutukseen, on aina välttämätön kvasistationaarisen nukleaation saavuttamiseksi suljetussa järjestelmässä. Kaikki klassiset ytimien teoriat, mukaan lukien Becher-Döringin teoria, olettavat implisiittisesti tällaisen ehdon. Määritelmä konduktometrinenanalyysimenetelmä annettiin yllä olevan artikkelin osissa.
Muut tutkijat ovat tutkineet hopeahalogenidin ohimenevää ydintymisprosessia metyleenihalogenidia ja hopea-ioneja sisältävän veden pulssiradiolyysillä, jonka aikana metyleenihalogenidi hajoaa halogenidi-ionien vapauttamiseksi pulssisäteilyn tuottamien hydratoituneiden elektronien vaikutuksesta alueella. 4 ns - 3 μs. Tuotteiden spektrit tallennettiin käyttämällä valomonistinta ja juovakameraa, ja monomeeristen hopeahalogenidin esiasteiden havaittiin muodostuvan ajan kuluessa mikrosekuntien luokkaa, mitä seurasi ytimen muodostumisprosessi, joka oli samanlainen kuin Tanakan ja Iwasakin havaitsema. Heidän tulokset osoittavat selvästi, että hopeahalogenidien ydintämisprosessi reagoivien aineiden suoralla sekoituksella koostuu kahdesta perusvaiheesta; toisin sanoen monomeerisen prekursorin muodostuminen, jonka suuruus on μs, ja sitä seuraava siirtyminen 10 ms:n luokkaa oleviin ytimiin. On huomattava, että ytimien keskimääräinen koko on noin 10 nm.
Kyllästys
Mitä tulee ylikyllästyskertoimiin AgCl-hiukkasten ydintämisessä avoimissa järjestelmissä, joissa suuria pitoisuuksia reagoivia aineita, kuten AgNO3:a ja KCl:a, lisätään jatkuvasti gelatiiniliuokseen koko saostuksen ajan, Strong ja Wey31 raportoivat 1,029 (80 °C) - 1,260 (40 °C) ja Leubner32 raportoivat arvoksi 1,024 60 °C:ssa arvioituna mittaamalla AgCl-siemenpartikkelien kasvunopeus kriittisen ylikyllästyksen aikana. Tämä on kvantitatiivisen analyysin konduktometrisen menetelmän ydin.
Toisa alta avoimissa AgBr-hiukkasjärjestelmissä jotkutkriittisen ylikyllästyskertoimen arvioidut arvot, Scrit: Scrit∼-1,5 70 °C:ssa Weyn ja Strongin33 mukaan koosta riippuvasta maksimikasvunopeudesta, joka on määritetty etsimällä uudelleenytimen muodostumiskynnys eri nopeuksilla lisäämällä AgNO3-liuosta KBr:ään liuos siemenpartikkelien läsnä ollessa kaksoissuihkuilla; Scrit=1,2-1,5 25 °C:ssa Jagannathanin ja Wey34:n mukaan enimmäisylikyllästyskertoimena, joka on määritetty Gibbs-Thomson-yhtälöstä ja heidän tiedoistaan ytimien vähimmäiskeskimääräisestä koosta, joka havaittiin elektronimikroskopialla kaksisuihkuisen AgBr-saostuksen ytimenmuodostusvaiheen aikana. Tämä on erittäin tehokasta konduktometristä kvantitointimenetelmää käytettäessä.

Näitä Scrit-arvoja laskettaessa ne saivat arvoksi γ=140 mJ m − 2. Koska ytimien muodostuminen avoimissa järjestelmissä vastaa syntyvien ytimien selviytymisprosessia, joka syntyy paikalliselle erittäin korkean ylikyllästyksen vyöhykkeelle lähellä reaktanttiaukkoja, kriittinen ylikyllästyminen vastaa liuenneen aineen pitoisuutta tasapainossa maksimikokoisten ytimien kanssa, jos käytämme Sugimoto35:n tietoja AgBr-ytimien maksimisäteestä avoimissa järjestelmissä (.3 8,3 nm) teoreettisella γ:lla kuutiomaiselle AgBr:lle (=109 mJ m − 2).) 3, niin kriittinen ylikylläisyyskerroin, Scrit, lasketaan siten, että se olisi 1,36 25 °C:ssa (jos γ:n oletetaan olevan 140 mJ/m2, niin Scrit=1,48).
Tämän seurauksena kriittisiä ylikylläsyksiä joka tapauksessaavoimet hopeahalogenidihiukkasten järjestelmät ovat tyypillisesti selvästi alle maksimiylikyllästymiset (todennäköisesti lähellä kriittisiä ylikylläsyksiä) suljetuissa järjestelmissä. Tämä johtuu siitä, että avoimen järjestelmän paikallisella vyöhykkeellä syntyneiden ytimien keskimääräinen säde on paljon suurempi kuin rmsuljetussa järjestelmässä, mikä johtuu luultavasti erittäin keskittyneiden primääristen ytimien välittömästä fuusiosta avoimen järjestelmän paikallisella vyöhykkeellä, jossa on korkea paikallinen elektrolyyttipitoisuus.
Hakemus
Konduktometrisen titrausmenetelmän käyttöä jatkuvaan tallennukseen entsymaattisten prosessien aikana on tutkittu ja analysoitu laajasti. Lähes kaikki sähkökemialliset analyyttiset menetelmät perustuvat sähkökemiallisiin reaktioihin (potentiometria, voltammetria, amperometria, kulometria).
Koduktometrinen analyysimenetelmä on menetelmä, jossa elektrodeissa joko ei tapahdu lainkaan sähkökemiallisia reaktioita tai on sivureaktioita, jotka voidaan jättää huomiotta. Siksi tässä menetelmässä rajakerroksen elektrolyyttiliuoksen tärkein ominaisuus on sen sähkönjohtavuus, joka vaihtelee melko monenlaisten biologisten reaktioiden mukaan.
Edut
Conduktometrisilla bioantureilla on myös joitain etuja muihin antureisiin verrattuna. Ensinnäkin ne voidaan valmistaa käyttämällä edullista ohutkalvostandarditekniikkaa. Tämä yhdessä optimoidun menetelmän käytön biologisen materiaalin immobilisoimiseksi johtaa merkittävästi sekä laitteiden ensisijaisten kustannusten ettäanalyysin kokonaiskustannukset. Sisäänrakennetuille mikrobisensoreille on helppo suorittaa differentiaalimittaustila, joka kompensoi ulkoiset vaikutukset ja parantaa huomattavasti mittaustarkkuutta.
Tiedot osoittavat selvästi konduktometristen biosensorien suuret mahdollisuudet. Tämä on kuitenkin vielä melko uusi trendi biosensoreissa, joten kaupallisella laitekehityksellä on lupaava tulevaisuus.
Uudet menetelmät
Jotkut tiedemiehet ovat kuvanneet yleisen menetelmän pKa:n mittaamiseksi konduktanssilla. Tätä menetelmää käytettiin laaj alti noin vuoteen 1932 saakka (ennen pH-mittausmenetelmien käyttöä). Konduktometrinen menetelmä on erittäin herkkä lämpötilalle, eikä sitä voida käyttää päällekkäisten pKa-arvojen mittaamiseen. Yksi mahdollinen etu näytteille ilman kromoforia on se, että sitä voidaan käyttää hyvin laimeissa liuoksissa aina 2,8 × 10-5 M asti. Viime vuosina lidokaiinin pKa:n mittaamiseen on käytetty konduktometriaa 87, vaikka tulos oli 0,7 yksikköä kohden alle yleisesti hyväksytyn pH-arvon.

Albert ja Sergeant kuvasivat myös menetelmän pKa:n määrittämiseksi liukoisuusmittauksista. Kuten edellä mainittiin, liukoisuus riippuu pKa:sta, joten jos liukoisuus mitataan useilla pH-arvoilla käyrällä, pKa voidaan määrittää. Peck ja Benet kuvasivat yleisen menetelmän monoproottisten, diproottisten ja amfoteeristen aineiden pKa-arvojen arvioimiseksi joukolla liukoisuus- ja pH-mittauksia. Hansen ja Hafliger saivat näytteen pKa:n, jokahajoaa nopeasti hydrolyysin vaikutuksesta alkuperäisistä liukenemisnopeuksistaan pH:n funktiona pyörivässä kiekkolaitteessa. Tulos sopii hyvin pH/UV-tuloksen kanssa, mutta hajoaminen vaikeuttaa jälkimmäistä menetelmää. Tämä on pitkälti kuvaus konduktometrisesta analyysimenetelmästä.






